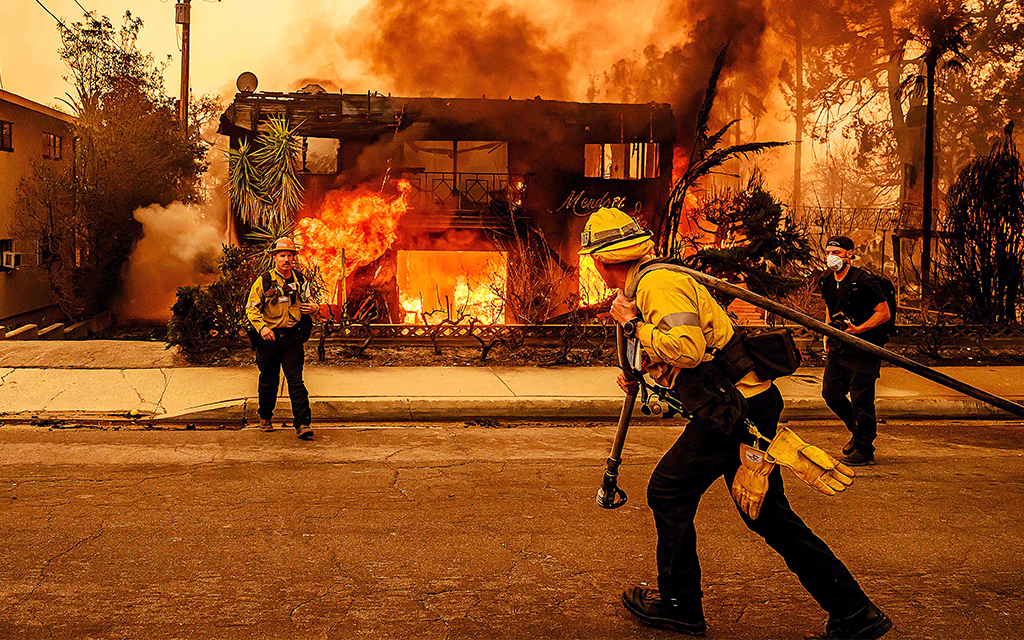I gensaxens födelsestad Umeå pågår just nu en studie för att med hjälp av Crispr-tekniken hitta ett botemedel mot en ärftlig och dödlig sjukdom.

Text: Jill Bederoff, Dagens industri. Publicerad i Världen Om. ©2025 Bonnier News Business. Alla rättigheter förbehållna.
Vad handlar artikeln om?
I Norr- och Västerbotten finns en ärftlig sjukdom som kallas för Skelleftesjukan eller Ärftlig transtyretinamyloidos, som innebär inlagring av olösliga proteinkomplex i kroppens vävnader.
Sjukdomen är mycket allvarlig och enligt Socialstyrelsen lever cirka 450 svenskar med sjukdomen i dag. Källa: Neuroförbundet
I Umeå är man extra stolt över den franska Nobelpristagaren Emmanuelle Charpentier eftersom hon verkade vid stadens universitet när hon 2012 upptäckte Crispr-Cas9, det som i dagligt tal kallas gensaxen.
”När hon var här och jobbade var en granne, som är mikrobiolog, på besök och berättade om hennes forskning. Det blev snack om vad jag som läkare trodde man kunde ha den till. Mitt svar var att det var krångligt och troligen inte skulle gå att använda till något avgörande i människokroppar under min yrkesverksamma tid”, säger Björn Pilebro, biträdande universitetslektor och kliniker på kardiologen i Umeå.
I dag, drygt ett decennium senare, vet han bättre. Det var mitt under coronapandemin som ett mejl från Intellia Therapeutics damp ned i hans inbox, bolaget som grundats av bland andra den amerikanska forskaren Jennifer Doudna som delade Nobelpriset för Crispr-Cas9 med Emmanuelle Charpentier.
”De ville att vi skulle vara med i en studie för att utveckla ett Crispr-baserat läkemedel för transtyretinamyloidos, vars ärftliga form i Sverige ofta kallas Skelleftesjukan. Men just då, när det var kaos och sjukhuset var nedstängt, bad jag att få återkomma. Så vi var inte med hela vägen från projektstart, England och Nya Zeeland hade redan startat när vi kom igång.”

i Umeå. Foto: Klas Sjögren
Lika obekant Björn Pilebro vid tidpunkten var med att jobba med Crispr i praktiken, lika bekant var han med att jobba med Skelleftesjukan.
”Jag har nog varit prövare i läkemedelsstudier i 15 år eftersom vi har den här befolkningen med ärftlig transtyretinamyloidos. Det finns en form av transtyretinamyloidos som inte är ärftlig, men den har, då den främst drabbar äldre, inte uppmärksammats i större grad förrän de senaste åren. Majoriteten av alla svenskar med ärftlig sjukdom, som det forskats kring i många år, bor i Norr- och Västerbotten.”
Skelleftesjukan är en relativt vanlig sjukdom i norra Sverige. Den orsakas av en förändring av arvsanlaget för proteinet transtyretin. Men trots att en enda mutation orsakar sjukdomen är sjukdomsbilden mellan patienterna väldigt varierande. Vissa som bär på anlaget utvecklar sjukdomen så tidigt som i 25-årsåldern, medan andra aldrig blir sjuka.
”Transtyretinamyloidos är en sjukdom där transtyretin, ett protein som vi alla har i blodet, istället för att stanna kvar i blodet och göra det det ska, antar fel form och klumpar ihop sig i olösliga strängar som lägger sig i vävnader och förstör dem. Hjärtat blir tjockare och styvare, och till slut kan det inte pumpa alls. Men vid den ärftliga formen av sjukdomen har både kroppens nerver och magtarmfunktionen ofta förstörts innan detta sker.”
Det finns flera godkända läkemedel som används mot Skelleftesjukan, både i Sverige och internationellt. Såväl tabletter som injektioner.
”Kombinationen av att man kan röntga och hitta de här inlagringarna och läkemedel samt att vi har en hel massa ganska friska 75-åringar, gör att intresset för den icke ärftliga formen av sjukdomen också ökat.”
Samtidigt finns det flera anledningar till att Intellia Therapeutics fokuserar på Skelleftesjukan i sin utveckling av Crispr-baserade läkemedel.
”De behandlingar som kommit de senaste åren stänger av produktionen av protein genom att påverka steget mellan gen och protein, det som kallas RNA. Sådana studier har vi varit inblandade i sedan 2010. Det var väl därför vi tillfrågades om vi ville vara med i det här projektet. Egentligen gör Crispr-Cas9 samma sak som visat sig funka med de två andra läkemedelsgrupperna som ger sig på RNA.”
Intellias Fas I-studie med 72 patienter med ärftlig amyloidos har visat att behandlingen verkar pålitligare än nuvarande behandlingsalternativ.
”Med de mediciner som vi har använt hittills har vi sett att det finns några patienter som svarar sämre.”
Administrationen är ett annat område. Med de tidigare behandlingarna har patienterna gått från injektioner var tredje vecka till var tredje månad. Med Crispr-tekniken räcker det med en spruta, en gång.
”Med Crispr-tekniken räcker det med en spruta, en gång.”
Björn Pilebro, överläkare och bitr. universitetslektor vid Umeå universitet
Innan man klipper bort en gen från en människa är det självklart viktigt att förstå vilka negativa konsekvenser det kan få.
”Den lilla oro som vi har, men som blir mindre för varje år som går, är att transtyretin är ett evolutionärt välbevarat protein. I inget släkte har det slagits ut, så något essentiellt gör det. Samtidigt har vi inte sett någon negativ effekt hos patienter som behandlats med de godkända preparaten i snart 15 år nu. Det blir tryggare och tryggare, och är ytterligare en anledning till att Intellia fokuserat på Skelleftesjukan.”
Hittills finns det endast ett godkänt Crispr-baserat läkemedel i världen. Det är Casgevy, för behandling av en ärftlig blodsjukdom.
”I denna behandling plockar man ut celler från patienten, ’lagar’ dem och sprutar in dem igen. En genetisk reparation och ett jättesnyggt användningsområde för Crispr. I den studie jag är med i handlar det mer om genetisk amputation, att paja genen helt enkelt. Det är ganska burdust.”
Det är just i behandlingar utanför kroppen som Crispr-tekniken främst kommer att synas de kommande tio, femton åren, tror Björn Pilebro.
”Som att redigera blodstamceller, laga existerande vanligare mutationer eller som man gjort i det som heter Car-T där Crispr-teknik används för att programmera om vita blodkroppar att ge sig på cancer.”
Efter en avslutad fas 1-studie på 72 patienter med Skelleftesjukan med positiva resultat, påbörjades en fas 3-studie, Magnitude, med 765 patienter i höstas.
”Det är en stor placebokontrollerad studie med runt tre års uppföljning. Efter det får man räkna med ett år innan datainsamlingen och sammanställningen är klar. Sedan tar det upp till ett år innan de olika läkemedelsverken ger sin syn på produkten.”

Denna text publicerades ursprungligen i det tryckta magasinet Världen Om juni 2025.
Läs fler artiklar från samma nummer här.
Så här jobbar Världen Om med kvalitetsjournalistik: Vi väljer ut artiklar. analyser, data och intervjuer från The Economist som täcker in geopolitik, vetenskap, livsstil, affärer och kultur. The Economist har funnits sedan 1843 för att "stärka kampen för intelligent upplysning i syfte att motverka okunskap som hindrar framsteg och utveckling."