Kina ligger på andra plats, efter USA, bland världens ledande utvecklare av nya läkemedel. Förra året genomförde kinesiska bolag nästan en tredjedel av alla kliniska prövningar globalt. Det är en ökning från låga 5 procent för ett decennium sedan (se diagram 1). Landet är också på väg att bli ledande inom flera viktiga forskningsområden, bland annat cancer.

Ur The Economist, 23 november 2025, översatt av InPress. ©2026 The Economist Newspaper Limited. Alla rättigheter förbehållna.
Vad handlar artikeln om?
Fram tills helt nyligen var Kinas läkemedelsindustri mest känd för att tillverka generika och för att vara underleverantör åt företag i väst. Nu ligger Kina på andra plats bland världens läkemedelsutvecklare, inte minst inom cancer- och fetmabehandling. Det är en utmaning för Big Pharma, men kan samtidigt få stor betydelse för patienter i fattiga länder. För kinesiska läkemedelsbolag väntar tre avgörande utmaningar: att utveckla nya behandlingar som fungerar, ta sig in på nya marknader med dem och efterleva regleringskraven.
Kina ligger på andra plats, efter USA, bland världens ledande utvecklare av nya läkemedel. Förra året genomförde kinesiska bolag nästan en tredjedel av alla kliniska prövningar globalt. Det är en ökning från låga 5 procent för ett decennium sedan (se diagram 1). Landet är också på väg att bli ledande inom flera viktiga forskningsområden, bland annat cancer.
Investerarna har noterat detta. Aktierna i kinesiska bioteknikföretag steg med 110 procent fram till december i fjol, vilket är mer än tre gånger så mycket som deras amerikanska motsvarigheter.
Under större delen av förra århundradet dominerades läkemedelsforskningen av stora europeiska och amerikanska bolag – gruppen kallas ofta ”big pharma”. Så är det inte längre. De här bolagen står nu inför ett scenario där ett stort antal patent löper ut. Läkemedel som förväntas generera mer än 300 miljarder dollar i totala intäkter under de kommande sex åren blir av med sitt patentskydd 2030. För att kompensera för bortfallet letar amerikanska och europeiska bolag världen över efter lovande molekyler. Allt oftare hittar de dem i Kina.
Tidpunkten är inte den bästa. USA vill minska sitt beroende av kinesiska leveranskedjor, eftersom handelskriget bara pausats tillfälligt. Amerikanska tjänstemän oroar sig exempelvis redan över att Kina tagit kontroll över vissa aktiva läkemedelsingredienser. Och rykten cirkulerar om att Vita huset planerar att slå till mot den kinesiska läkemedelsindustrin – även om det hittills inte har hänt så mycket.
När nästa generations läkemedel ska utvecklas är det dock troligt att amerikanska läkemedelstillverkare och patienter kommer att bli mer – inte mindre – beroende av kinesiska innovationer.
Det finns mycket som pekar i den riktningen. I maj gick Pfizer, det största amerikanska läkemedelsbolaget, med på att betala 1,25 miljarder dollar i avgifter till det kinesiska bioteknikföretaget 3SBio för rättigheterna att tillverka och sälja ett experimentellt cancerläkemedel utanför Kina, förutsatt att det godkänns. Månaden därpå ingick den brittiska konkurrenten GlaxoSmithKline ett avtal värt 500 miljoner dollar med det kinesiska företaget Hengrui om en behandling av lungsjukdomar.
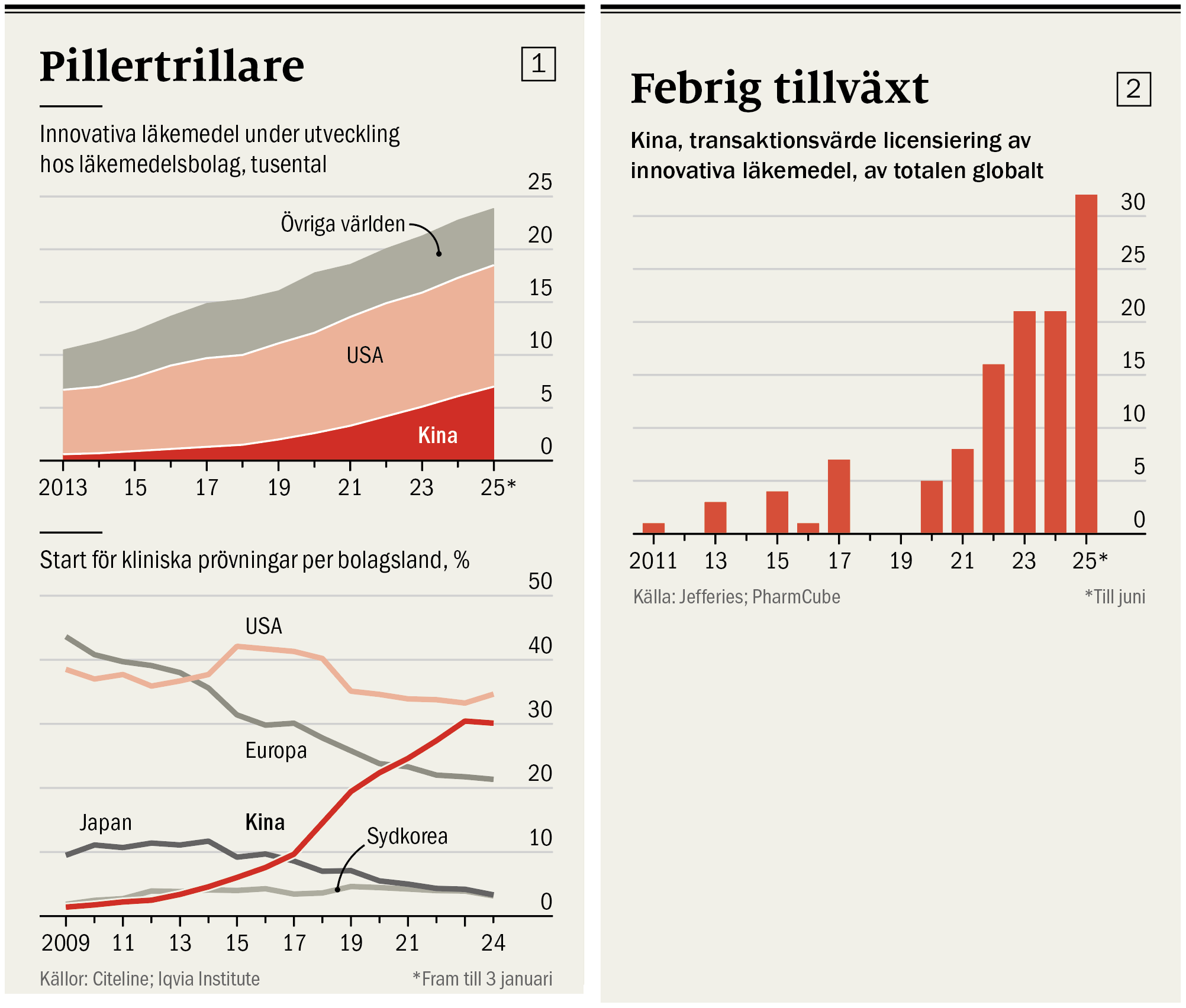
Man har också option att köpa ytterligare elva läkemedel, sammantaget värderade till hela 12 miljarder dollar. Allt beror på om Hengrui lyckas nå vissa milstolpar i utvecklingen. Den här typen av avtal är inte längre särskilt ovanliga. Under första halvåret i år hade nästan en tredjedel av alla globala licensavtal som ingicks av stora läkemedelsbolag kinesiska företag som motpart – andelen har fyrdubblats sedan 2021 (se diagram 2).
Fram tills helt nyligen var Kinas läkemedelsindustri mest känd för att tillverka generiska läkemedel, leverera ingredienser och genomföra studier åt företag i väst. Under det senaste decenniet har industrin fått en nystart. Processerna för godkännande har effektiviserats, prioriterade granskningar genomförs när det gäller läkemedel för behandling av svåra sjukdomar och regelverket anpassas till internationella standarder.
Antalet anställda hos den kinesiska läkemedelsmyndigheten fyrfaldigades mellan 2015 och 2018, och det tog bara två år att beta av en kö med 20 000 nya läkemedelsansökningar. Tiden för att säkra godkännande för kliniska prövningar på människor kortades från 501 till 87 dagar. Och produktionen av nya läkemedel ökade kraftigt. 2015 godkände Kina endast elva behandlingar, främst västerländska importprodukter. 2024 hade den siffran stigit till 93, varav 42 procent var utvecklade inom landet.


Parallellt med de här reformerna har insatser gjorts för att locka tillbaka studenter och yrkesverksamma som har studerat eller arbetat utomlands. Många av Kinas ”havssköldpaddor”, som de här återvändarna skämtsamt kallas, tar med sig erfarenheter av att bygga upp bioteknikföretag och hantera investerare och tillsynsmyndigheter tillbaka till landet. Deras entreprenörsanda har fått stöd av regelverk som gör det lättare att hämta in investeringskapital och att få bolag noterade på Hongkong-börsen.
Det finns gott om tecken på att detta är ett framgångsrecept. I november 2019 blev det kinesiska bioteknikföretaget BeOne Medicines, tidigare känt som BeiGene, det första lokala företaget som fick godkännande från den amerikanska tillsynsmyndigheten Food and Drug Administration, FDA, för ett läkemedel för cancerbehandling. Detta följdes av fler godkännanden. Men något riktigt stort inträffade i september förra året när ett läkemedel för behandling av lungcancer, utvecklat av det lilla kinesiska bioteknikföretaget Akeso Bio, uppvisade bättre resultat i kliniska studier än Keytruda, Mercks banbrytande behandling.
Vad ligger bakom de kinesiska läkemedelsbolagens snabba uppgång? Det första svaret handlar om att de var snabba med att ställa om för att kunna producera ”snabba efterföljare”, som förbättrar säkerheten hos eller leveransen av befintliga läkemedel. De kunde sedan gå vidare till pionjärläkemedel med nya mål (som ett protein eller en gen kopplad till sjukdom) eller mekanismer (som kan blockera eller stärka ett måls funktion).
”Snabba efterföljare” och pionjärbehandlingar utgör nu mer än 40 procent av branschens pipeline, enligt intressant forskning från Zimeng Chen och hans team vid Tsinghua University i Peking, som publicerades 2024 i den vetenskapliga publikationen Nature Reviews Drug Discovery. Wang Xingli från den kinesiska läkemedelstillverkaren Fosun Pharma säger, att arbetet med snabba efterföljarläkemedel gav Kinas industri ”modet att gå vidare till pionjärläkemedel”.
En andra förklaring handlar om hur snabba, omfattande och billiga andra processer är. För kinesiska företag kan det gå ungefär dubbelt så snabbt att utveckla ett läkemedel från upptäckt till inledande kliniska prövningar på människor jämfört med genomsnittstiden för branschen globalt. De kliniska prövningarna på människor, som normalt är den långsammaste fasen i utvecklingen av ett nytt läkemedel, går också snabbare.
Ett stort urval av patienter gör rekryteringen enklare och ett omfattande nätverk av studiecenter bidrar också till att påskynda processen. Den här modellen har visat sig vara särskilt användbar för att utveckla ADC-läkemedel, en ny behandlingsklass som verkar ha extra god effekt vid cancerbehandling. En chef hos ett stort läkemedelsbolag säger att Kina är attraktivt eftersom det finns många företag som experimenterar: ”Man kan välja vinnarna och öka oddsen för godkännande”.
Cancer är fortsatt ett centralt fokus för kinesiska bolag, men de satsar också på nya områden. Viktminskningsläkemedel är ett hett område. Patenten för semaglutid – den aktiva ingrediensen i Wegovy och Ozempic, de mycket populära viktminskningsbehandlingarna från den danska läkemedelsjätten Novo Nordisk – kommer att löpa ut i Kina nästa år. Därför tävlar många bolag om att ta fram generika. Men lokala bolag gör mer än att bara kopiera. Analysföretaget Bloomberg Intelligence bedömer att det finns 160 nya läkemedel mot fetma som håller på att utvecklas runt om i världen, ungefär en tredjedel av dem kommer från Kina.
Även om landet är världens näst största läkemedelsmarknad efter USA, är det fortfarande svårt att uppnå lönsamhet där. Konsultföretaget McKinsey uppskattar att landets försäljning av receptbelagda läkemedel uppgick till cirka 125 miljarder dollar 2023, en sjättedel så mycket som i USA. Merparten av försäljningen utgörs fortfarande av generika. Nya läkemedel svarar endast för en femtedel av marknaden, en andel som kan ha stigit till en tredjedel 2028.
Trots detta kommer marknaden fortsatt att vara mycket priskänslig. De flesta köp omfattas av statliga försäkringar och sjukhusens efterfrågan kan slås ihop till samlade inköp. Det gör att bolagen måste konkurrera om att vinna anbud. Läkemedelsbolagen måste ofta sänka priserna med hälften eller mer för att nå ut till större patientgrupper. Annars får de nöja sig med en betydligt mindre privat marknad.
Det förklarar varför USA och andra utländska marknader är så attraktiva. Den vanligaste vägen att ta sig in på de här marknaderna är via licensavtal med företag i väst. Vissa kinesiska företag vill nu ha en större del av kakan. En växande modell är ”NewCo”, där ett bioteknikföretag etablerar ett juridiskt separat bolag i USA, ofta med stöd av utländska investerare, och knoppar av lovande tillgångar till detta bolag. Den kinesiska läkemedelsindustrin är mycket attraktiv för bolag i väst. Marknadsvärdet för börsnoterade kinesiska bioteknikföretag motsvarar 15 procent av värdet för deras amerikanska motsvarigheter. I licensaffärer är förskottsbetalningarna typiskt sett två tredjedelar lägre än i motsvarande globala transaktioner, och transaktionernas totala storlek värderas till omkring hälften.

National Security Commission on Emerging Biotechnology (NSCEB).
Foto: www.newamerica.org
En annan fördel med ”NewCo”-modellen är att den kan bidra till att minska en del av den politiska oron kring den kinesiska läkemedelsindustrin utomlands. Det finns dock gott om andra orosmoment, inte minst vad gäller dataintegritet. Integritetsregler och relaterade granskningsprocesser gör det svårare att dela patientdata från kliniska studier. Och FDA har intagit en strikt hållning till att godkänna läkemedel baserat på studier som enbart utförts i Kina. I juni stoppade myndigheten alla nya kliniska prövningar som exporterade amerikaners genetiska data till Kina. En rapport från en kongresskommitté, där den tidigare Google-chefen Eric Schmidt ingick, publicerad i april 2025, varnar för att Kinas styrka inom läkemedelsupptäckter, i kombination med landets framsteg på AI-området, snart skulle kunna leda till att de kinesiska bolagen går om de amerikanska. Han och andra oroar sig för säkerhetsriskerna vid skärningspunkten mellan läkemedel och bioteknik.
Men det finns också anledning till försiktig optimism. Mer konkurrens leder till att fler behandlingar utvecklas, med lägre prislappar. För patienter som länge nekats tillgång till avancerade läkemedel, kan Kinas uppgång hjälpa till att öka tillgängligheten. Det skulle få stor betydelse för patienter i fattiga länder. För kinesiska läkemedelsbolag väntar tre avgörande utmaningar: att utveckla nya behandlingar som fungerar, ta sig in på nya marknader med dem och efterleva regleringskraven.
Xingli Wang noterar att det tog ungefär ett sekel för de flesta läkemedelsjättar att nå dagens storlek. Baserat på detta tror han att Kinas läkemedelsindustri fortfarande befinner sig ”i en mycket tidig fas”.

Denna text publicerades ursprungligen i det tryckta magasinet Världen Om mars 2026.
Läs fler artiklar från samma nummer här.
Så här jobbar Världen Om med kvalitetsjournalistik: Vi väljer ut artiklar. analyser, data och intervjuer från The Economist som täcker in geopolitik, vetenskap, livsstil, affärer och kultur. The Economist har funnits sedan 1843 för att "stärka kampen för intelligent upplysning i syfte att motverka okunskap som hindrar framsteg och utveckling."